Harmonização do Consenso brasileiro (CBA) e o Internacional (ICAP) para o exame Autoanticorpos anti-célula (ANA HEp-2) em Imunofluorescência Indireta (HEp-2 IFI)
Esse informativo busca atualizar os médicos e os laboratórios que realizam o exame sobre as novas nomenclaturas. A sexta edição do Consenso Brasileiro de Autoanticorpos (BCA/HEp-2) foi publicado em 7 de setembro de 2022 no periódico Advances in Rheumatology. As diretrizes para pesquisa de utoanticorpos em células HEp2 manteve o foco nos processos de harmonização com o Consenso Internacional sobre Padrões ANA (ICAP), para preencher lacunas entre as duas classificações e discutir sobre temas importantes, com relação à classificação de padrões, que possuam repercussão no dia a dia para os clínicos que interpretam o teste.
O que foi discutido
- A classificação de padrões complexos anteriormente designados como padrões mistos.
- A sugestão de dividir a classificação do padrão de pontos discretos nucleares.
- A classificação do padrão AC-4a com configuração de fluorescência peculiar sugestiva de autoanticorpos anti-SS-A/Ro60.
- Indicação de notificação obrigatória do status da coloração do envelope nuclear.
O que foi alterado
- Foi adicionado a cada padrão o código alfanumérico correspondente, ao todo 30 padrões reconhecidos pelo ICAP, contribuindo para a consistência da informação científica a nível internacional.
- Foram reconhecidos todos os padrões classificados pelo ICAP, exceto o AC-28.
- Foram incluídos padrões adicionais não reconhecidos pelo ICAP. BCA/HEp-2 harmoniza este ponto criando códigos alfanuméricos preliminares para classificar os padrões ainda não reconhecidos pelo ICAP como o padrão nuclear pontilhado quase homogêneo (BAC-3) e o padrão nuclear grosseiro reticular (BAC-4).
- O BCA manteve o arranjo original de grupos de padrões (nuclear, nucleolar, citoplasmático, padrões mitóticos e complexos) na árvore de classificação, visando direcionar a atenção do analista para classificar os diferentes padrões com foco na positividade dos quatro compartimentos celulares (núcleo, nucléolo, citoplasma e aparelho mitótico) e células em divisão.
- Ao contrário da árvore de classificação ICAP, que inclui o grupo de padrões nucleolares dentro do nuclear, BCA prefere manter os padrões nucleolares em um grupo separado.
- Na definição da terminologia, o V CBA optou por manter a expressão “FAN” no nome do ensaio por ser a mais consagrada e reconhecida em documentos regulatórios e de fontes pagadoras. Porém, considerando-se a recomendação do ICAP para denominar a metodologia do teste como ensaio de Imunofluorescência indireta em células HEp-2 (HEp-2 IFA), o CBA adota o termo IFI HEp-2. Esta decisão visou a harmonização com o Designação recomendada pelo ICAP HEp-2 IFA usada em as
publicações mais recentes.
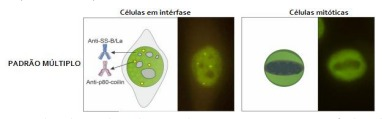
(resultante do padrão AC-21), com laudo AC-6/AC-21.
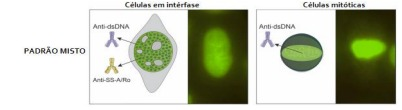
celular, não sendo possvel identificar o padrão de anticorpo correspondente. Para esses casos, o
Consenso BCA/HEp-2 recomenda a indicação no laudo das áreas com reatividade e a descrição da
fluorescência como um padrão misto no respectivo compartimento celular,
por exemplo, padrão nuclear misto.
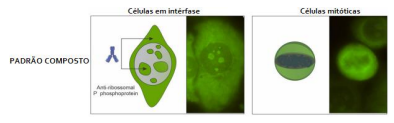
em diferentes compartimentos celulares.
Os padrões anteriormente únicos, passam a ser distintos. O VI BCA/HEp-2 recomenda a classificação dos padrões de pontos nucleares discretos em múltiplos pontos nucleares discretos (AC-6) e poucos pontos nucleares discretos (AC-7). Existem pelo menos três alvos antigênicos diferentes relacionados com o padrão de múltiplos pontos nucleares (AC-6).
- Sp100: Principal autoantígeno e consiste em uma proteína nuclear de 53 kDa relacionada com a ativação da transcrição celular.
- Proteína da leucemia promielocítica (PML): uma proteína supressora de transformação e crescimento celular, expressa em células de leucemia promielocítica, que co-localiza com Sp-100 em domínios nucleares (pontos), coexistindo em muitos casos no mesmo soro.
- Proteína 2 da matriz nuclear de 140 kDa (NXP-2), previamente identificada como autoantígeno MJ com diversas funções nucleares, incluindo metabolismo do RNA e manutenção da arquitetura nuclear. A NXP-2 recruta e ativa a proteína p53 regulando a senescência celular, e o autoanticorpo contra ela tem sido descrito como um importante marcador sorológico da dermatomiosite juvenil.
Critérios para laudo descritivo
A recomendação é que o relatório indique o nome do padrão seguido do código ICAP, bem como o título, como primeira informação. A partir daí, os padrões de fluorescência em cada compartimento celular devem ser declarados. O compartimento do envelope nuclear deve ser agregado ao relatório de ensaio, além dos demais compartimentos celulares: núcleo, nucléolo, citoplasma, aparelho mitótico e placa metafásica.
O VI BCA/HEp-2 também sugere que o laudo inclua os endereços eletrônicos BAC/HEp-2 e ICAP para consulta de relevância clínica e outras informações úteis (www.hep-2.com.br , www.anapatterns.org).
Como exemplo, segue modelo de laudo para o padrão NUCLEAR HOMOGÊNEO (AC-1).

Referências:
- Cruvinel, W.M., Andrade, L.E.C., Dellavance, A. et al. VI Brazilian consensus guidelines for detection of anti-cell autoantibodies on HEp-2 cells. Adv Rheumatol 62, 34 (2022). https://doi.org/10.1186/s42358-022-00266-z
- Damoiseaux J, von Mühlen CA, Garcia-De La Torre I, et al. International consensus on ANA patterns (ICAP): the bumpy road towards a consensus on reporting ANA results. Auto
Immun Highlights. 2016;7(1):1. doi:10.1007/s13317-016-0075-0
ÁRVORES DE CLASSIFICAÇÃO
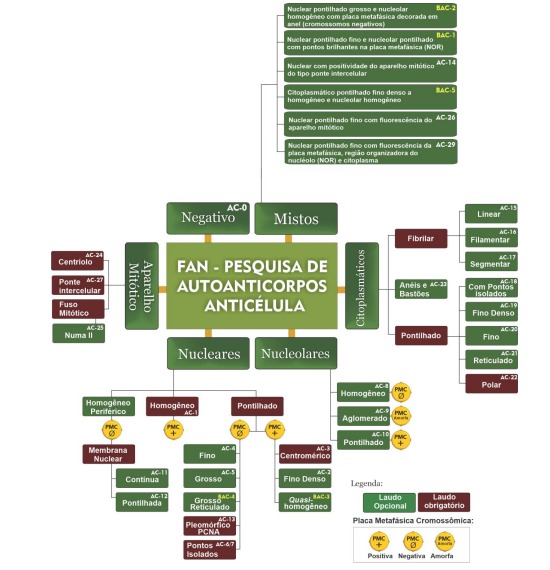
em https://www.hep-2.com.br/arvores-de-classificacao


